
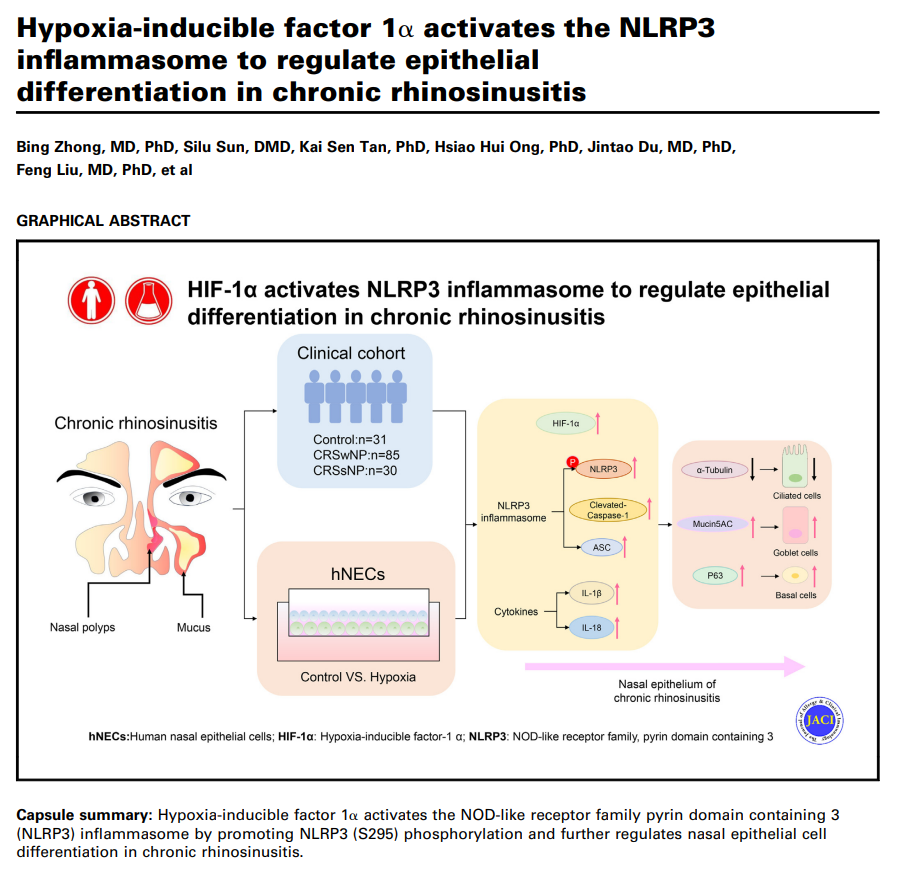
我院耳鼻咽喉头颈外科鼻科团队联合新加坡国立大学王德云教授团队及四川大学华西口腔医院李敬研究员团队在过敏医学顶级期刊Journal of Allergy And Clinical Immunology(IF:14.20, JCR学科类别“Allergy”28种期刊排名第1位)发表题为"Hypoxia-inducible factor 1α activates the NLRP3 inflammasome to regulate epithelial differentiation in chronic rhinosinusitis"的论著,首次揭示了在缺氧条件下,缺氧诱导因子(HIF)-1α的表达触发NLRP3炎性小体的激活,通过促进杯状细胞的分化并抑制纤毛细胞的表达,进而导致慢性鼻窦炎(CRS)上皮细胞的病理状态。这些结果进一步证实了低氧导致慢性鼻窦炎等上呼吸道炎症性疾病发病机制的复杂因素相互作用,并为进一步研究和潜在的治疗干预提供了新的干预途径,为寻求治疗CRS新的生物学靶点提供重要的理论依据,具有十分重要的临床转化意义。
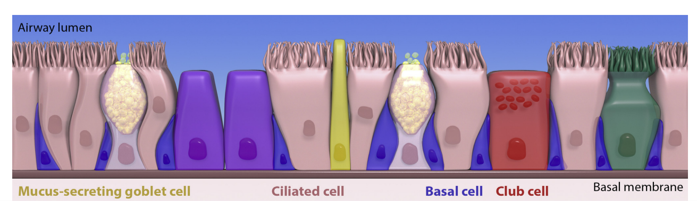
Hellings PW et.al. J Allergy Clin Immunol 2020
CRS是一类广泛存在于鼻黏膜的上呼吸道炎症性疾病,严重影响患者的生活质量并造成严重的经济负担。目前CRS分为伴有NPs的CRS (CRSwNP)和无NPs的CRS (CRSsNP)。鼻上皮主要由纤毛细胞、杯状细胞和基底细胞组成,作为上呼吸道的第一屏障,对外界环境的有害刺激起着物理屏障的作用。HIF-1α是一种在缺氧条件下上调的转录因子,其表达差异影响着细胞状态和炎性通路的开放;NLRP3炎性小体是一种多蛋白复合物,由NLRP3,caspase-1及ASC组成,能够调控成熟的促炎细胞因子IL-1β和IL-18的分泌,触发与炎症相关的各种生物学效应。然而,NLRP3炎性小体在缺氧反应的分子机制对CRS上皮细胞的影响仍不完全清楚。
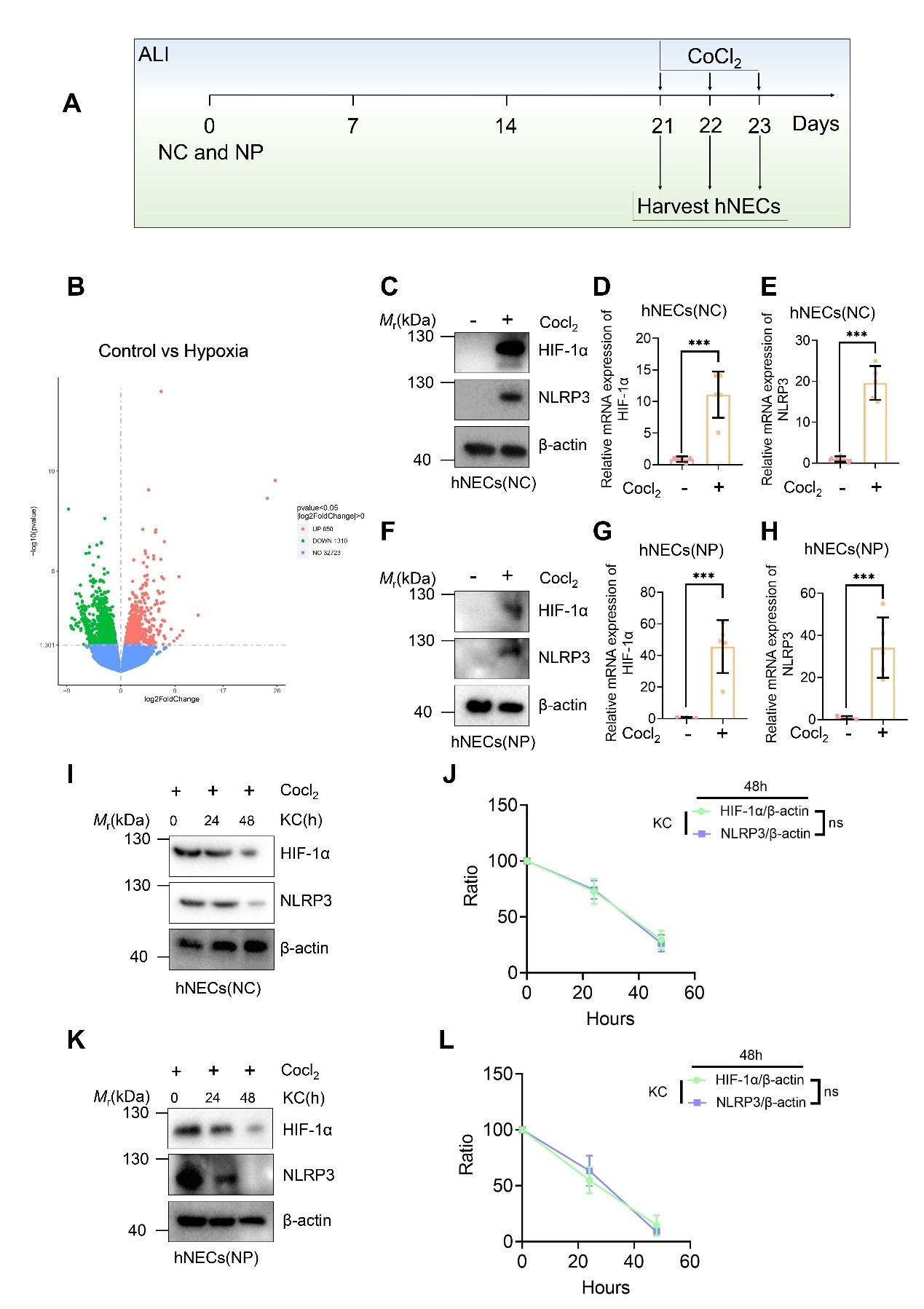
图1. HIF-1α和NLRP3在缺氧hNECc中的表达。
研究发现CRS组织(包括CRSsNP、EosCRSwNP和非EosCRSwNP)鼻黏膜中HIF-1α和NLRP3炎性小体的表达升高; 健康和CRSwNP患者的hNECs在短期缺氧模型中则揭示了HIF-1α可通过时间依赖性的方式降低NLRP3的激活(图1), 并能影响包括caspase-1、ASC在内的NLRP3炎性小体及下游炎性因子IL-1β和IL-18的表达。
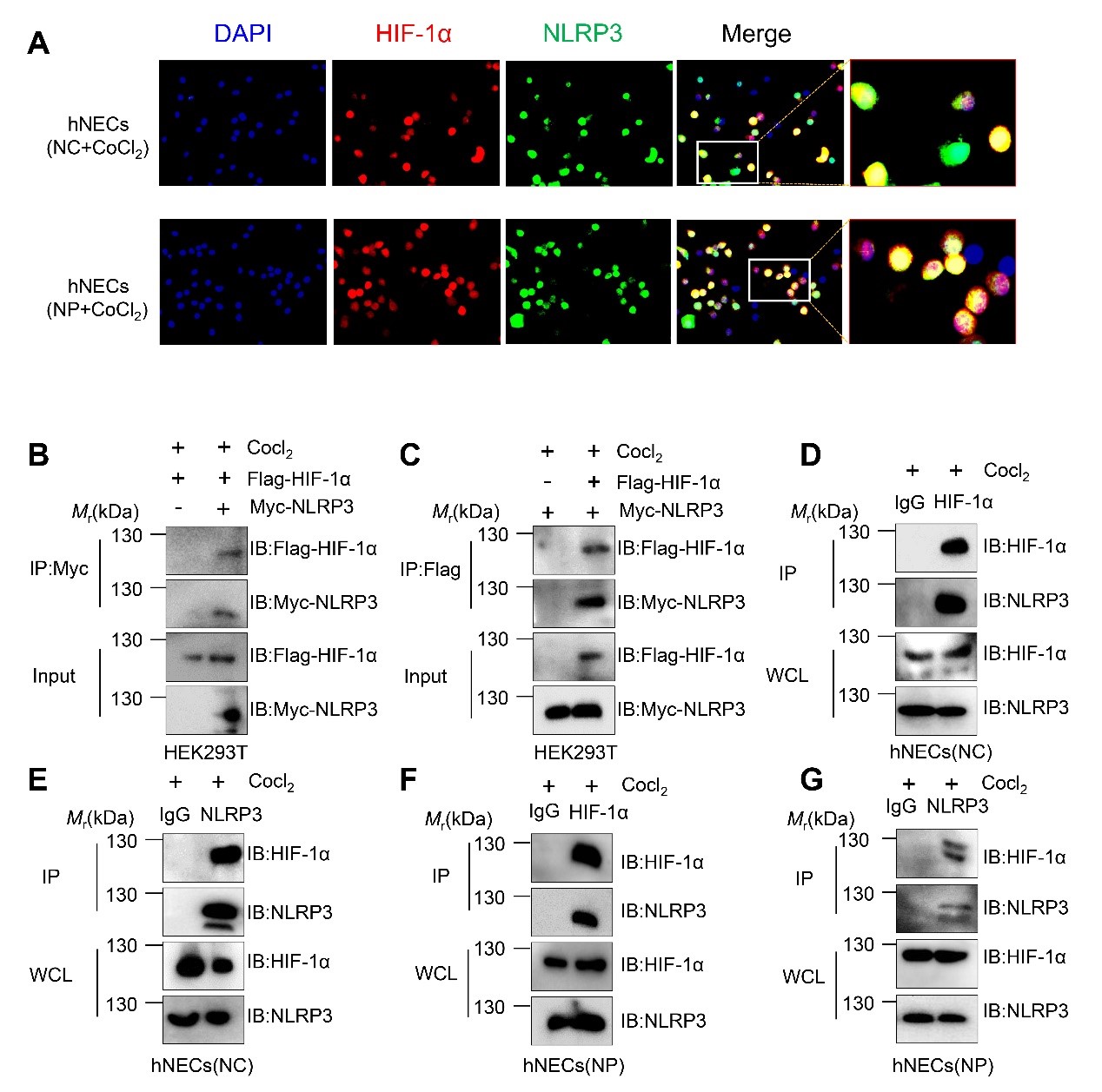
图2. 通过免疫荧光和Co-IP验证HIF-1α与NLRP3的关系。
HIF-1α具有与NLRP3结合的能力(HEK 293T细胞中及hNECs的外源性和内源性Co-IP)(图2), 并激活NLRP3 Ser295位点的磷酸化,促进NLRP3炎性体激活,进一步增强NLRP3与ASC和caspase-1的结合,并通过时间依赖性的方式减缓NLRP3的降解。
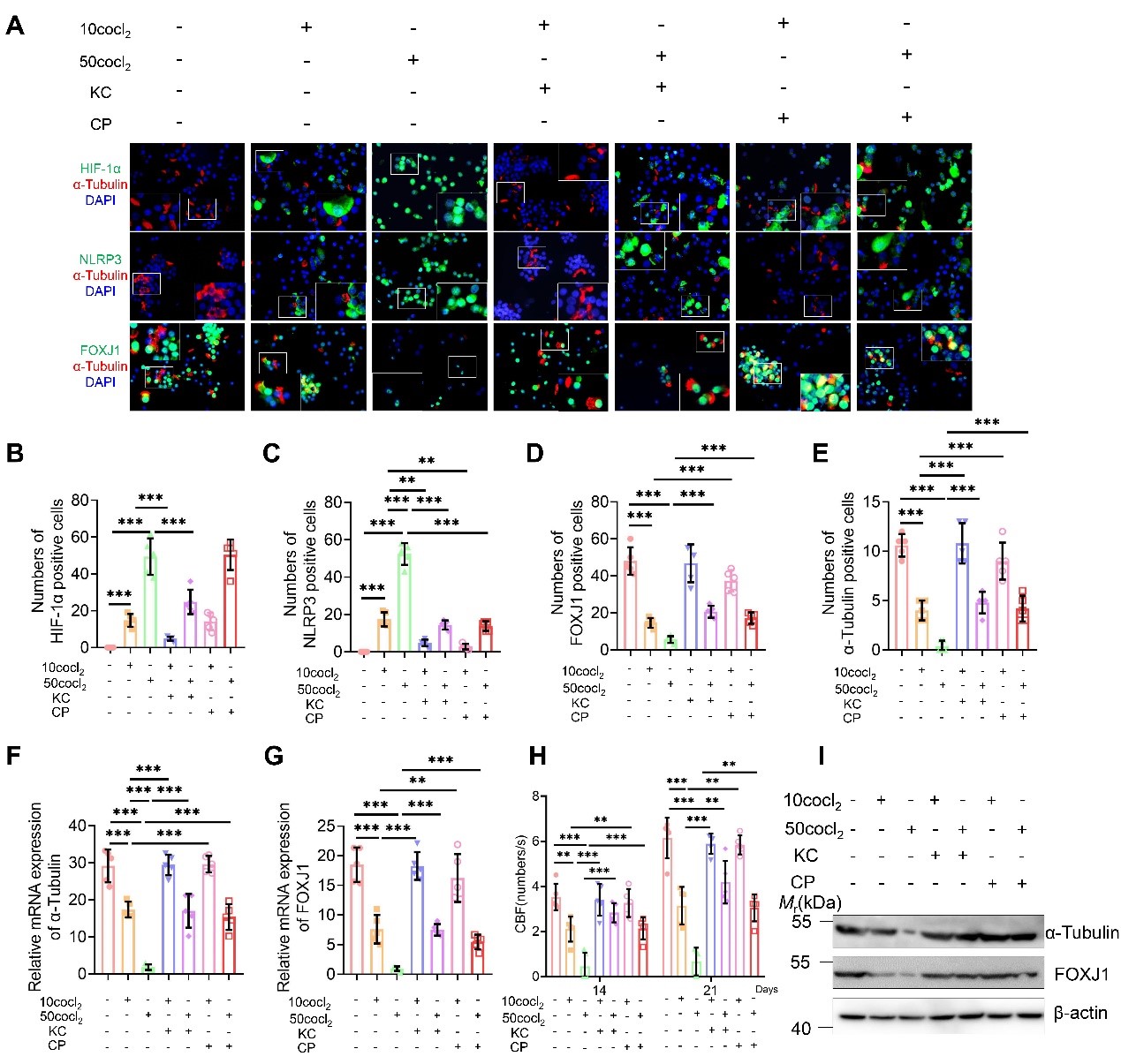
图3. HIF-1α促进NLRP3抑制纤毛细胞分化。
HIF-1α还可通过调控NLRP3的表达进一步减少hNECs中FOXJ1和α-Tubulin的水平进而抑制纤毛细胞的分化和功能(长期缺氧ALI模型) (图3)。

图4. HIF-1α通过激活NLRP3促进杯状细胞分化;HIF-1α可直接促进基底细胞的增殖。
HIF-1α能通过激活NLRP3炎性小体促进Mucin5AC的表达,进而促进hNECs杯状细胞分化; HIF-1α则可直接促进P63的水平,进一步提高基底细胞的增值能力(图4)。
我院耳鼻咽喉头颈外科钟兵助理研究员、四川大学华西口腔医院孙思露助理研究员为本论文的共同第一作者,新加坡国立大学王德云教授、刘静高级研究员、四川大学华西口腔医院李敬研究员为本文的通讯作者。
原文链接:
https://www.jacionline.org/article/S0091-6749(23)01201-0/fulltext