2021年9月20日,四川大学华西医院邵振华-颜微研究团队在Cell Research(IF:20.507)杂志发表了最新研究论文“Structural insights into sphingosine-1-phosphate recognition and ligand selectivity of S1PR3-Gi signaling complexes”。该研究成功解析了1-磷酸鞘氨醇受体S1PR3识别内源性配体S1P、第一代药物pFTY720、特异性配体CYM-5541及下游信号转导分子Gi蛋白的分子机制(图1),结合药理学实验手段揭示了S1PR3受体的激活机理及配体选择性机制。这是该研究团队继2021年9月15日发表的“Structures of signaling complexes of lipid receptors S1PR1 and S1PR5 reveal mechanisms of activation and drug recognition”论文后又一重要成果,两项研究相互补充,在人体脂质受体信号转导研究领域取得了重大进展。

脂质对于地球上的所有生命都是必不可少的,并且在能量储存和细胞膜的形成中起着至关重要的作用。1-磷酸鞘氨醇 (S1P) 作为一种天然存在的生物活性溶血磷脂,通过激活五种 G 蛋白偶联受体 (S1PR1–S1PR5) 来调节淋巴细胞运输、血管发育、内皮完整性和心率等基本生理过程。 S1PR 广泛分布于多种细胞类型,包括心血管、免疫和中枢神经系统中的细胞。 S1P-S1PR 信号传导与多种疾病的产生息息相关,靶向S1PR药物已被批准用于治疗多发性硬化症 (MS) 和溃疡性结肠炎(UC)。
由于五种亚型的S1PR序列高度同源,药物容易产生脱靶效应引起副作用。 例如,第一代药物芬戈莫德是S1PR1和S1PR5的双重受体调节剂,受体选择性低,且由于激动S1PR3,从而引起心动过缓、房室传导阻滞等临床不良反应。在自身免疫疾病药物开发上避免S1PR3可以有效减少心动过缓、房室传导阻滞等副作用,而针对S1PR3受体的特异性药物可以治疗缺血性心脏病。因此,了解 S1P-S1PR 信号传导机制并确定 S1PR 家族配体选择性的差异有助于开发安全性更高的药物,以控制 MS、心血管和自身免疫性疾病。
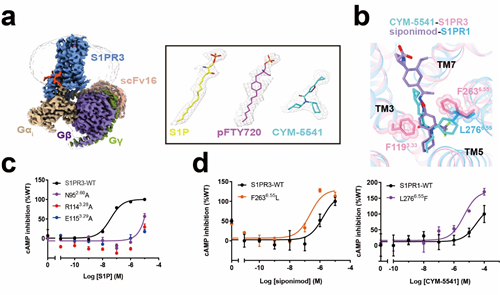
图1. S1PR3-Gi与不同配体的冷冻电镜三维结构及药理学实验
研究发现,对内源性配体S1P和第一代药物pFTY720采用相似的识别模式,包含极性头部识别口袋和疏水尾部识别口袋两部分,极性头部口袋的残基对受体的激活至关重要(图1c)。而特异性配体CYM-5541由于分子骨架较小只结合在正位口袋的疏水区域,有趣的是,之前报道S1P和CYM-5541可能占据不同的结合口袋,作者观察到CYM-5541的结合口袋与S1P的疏水烷基链重叠。
此外,作者观察到S1PR3与该家族的S1PR1整体结构和配体结合口袋都高度相似,但通过与S1PR1的结构进行比较和深入分析,作者发现了一些差异, 猜测TM6上6.55位置上的残基不同(S1PR3该位置为较大的苯丙氨酸,而S1PR1则为较小的亮氨酸)有助于受体识别各自的特异性配体(图1b),并结合药理学实验揭示了S1PR3和S1PR1对配体选择性的机制(图1d)。
综上所述,该论文在原子层面上详细阐释了脂质受体S1PR3的配体识别及配体选择性机制,该研究将为多发性硬化症、系统性红斑狼疮、恶性肿瘤、缺血性心脏病等疾病的药物开发和治疗奠定基础。
据悉,四川大学博士生赵畅、博士后程林、硕士毕业生汪微以及硕士生王贺莉为该论文的共同第一作者,邵振华研究员和颜微副研究员为共同通讯作者。冷冻电镜数据收集均获得了四川大学华西冷冻电镜平台、南方科技大学冷冻电镜中心的支持。该研究由四川省科技厅重点研发计划、科技部重点研发、国自然基金等项目资助完成。
邵振华-颜微研究团队围绕重大疾病靶标GPCR的功能性信号转导展开研究,发现了多个GPCR受体的新型别构位点,研究成果在Cell、Cell Research(*2)、Nature Chemical Biology、及Nature Communications 等国际期刊发表。