近日,我院胃癌中心胡建昆教授团队联合磁共振研究中心罗奎研究员团队在Advanced Science(IF:15.1)发表文章“Enzyme-Responsive Branched Glycopolymer-Based Nanoassembly for Co-Delivery of Paclitaxel and Akt Inhibitor toward Synergistic Therapy of Gastric Cancer”。该研究构建了一种新型组织蛋白酶B响应共载AKT抑制剂及紫杉醇药物递送系统,为胃癌治疗提供了新的策略。

胃癌是全球常见的恶性肿瘤之一,但目前治疗手段仍较局限。识别有效的治疗靶点并筛选相应的药物是开展胃癌精准治疗、提升患者远期预后的关键。研究发现蛋白激酶B(AKT)在多种肿瘤中高表达,且与肿瘤进展及治疗抵抗相关。研究团队首先探究了AKT作为胃癌治疗靶标的潜力,证实了AKT在胃癌组织中高表达,与胃癌不良预后相关,且AKT抑制剂capivasertib(CAP)与化疗药紫杉醇(PTX)能够协同杀伤胃癌细胞。
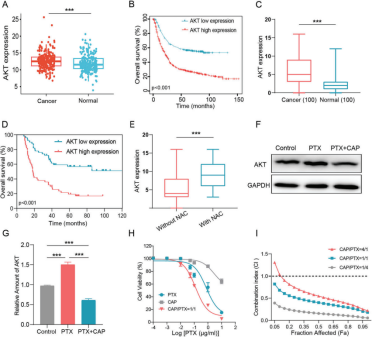
CAP是一种高效的泛AKT激酶抑制剂,对三种不同亚型的AKT具有较好的抑制作用。AKT抑制剂和化疗药物的组合可以协同促进肿瘤细胞凋亡。但由于水溶性差、毒副作用强,且缺乏肿瘤靶向性,导致其临床应用受限,因此需要开发有效的药物递送方式。在该项研究中,研究团队提出了一种创新方法,利用2-乳糖酰胺乙基甲基丙烯酰胺(LAEMA)作为支链糖聚合物的关键构建单元,设计和制备了组织蛋白酶B响应聚合物纳米颗粒前药系统共传递PTX和CAP,得到聚合纳米药物BPGP@CAP。该系统旨在精确靶向肿瘤细胞并控制PTX和CAP的释放。
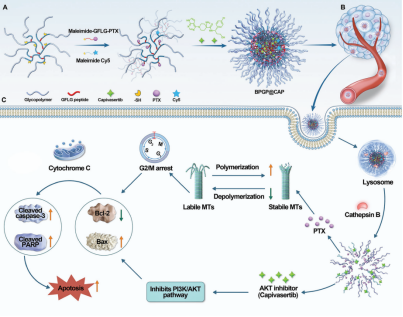
研究发现通过增强渗透滞留(EPR)效应,BPGP@CAP选择性地滞留在肿瘤组织上。BPGP@CAP被肿瘤细胞摄取后,在智能响应肿瘤细胞溶酶体中过表达的组织蛋白酶B后,精确释放PTX和CAP。释放的CAP抑制AKT及其下游通路,并与释放的PTX发挥协同抗肿瘤作用。同时,PTX和CAP由这种基于糖聚合物的药物递送系统中递送后,毒性显著降低。这种基于糖聚合物前药的酶响应纳米药物可用于化疗药PTX和靶向药物CAP的共递送,为胃癌治疗提供了一种新的方法。
我院胃癌中心胡建昆教授、磁共振研究中心罗奎研究员为通讯作者,胃癌研究室博士后宋小海、胸部肿瘤研究所蔡豪副研究员为共同第一作者。该研究工作得到了国家自然科学基金的支持。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202306230