2022年12月,我院移植免疫研究室刘敬平研究员团队在Journal of Controlled release(IF:11.467 )发表研究论文“Improving the circulation time and renal therapeutic potency of extracellular vesicles using an endogenous ligand binding strategy”。研究基于内源性配体结合策略,构建了可与内源血白蛋白结合的工程化EVs,提升其体内循环时间、肾脏分布及药物递送效率,为肾脏疾病的治疗研究提供了新思路。

急性肾损伤是一种临床常见危重症,具有较高的发病率和死亡率。肾损伤后不完全修复还可导致肾纤维化及慢性肾病,但目前仍缺乏有效的肾损伤修复疗法。近年来,随着病理机制和药物研发的进展,为肾损伤的治疗提供了多种候选药物如小分子化合物、蛋白质和核酸等。但这些药物往往存在体内半衰期短、缺乏肾脏靶向性等问题,而大量系统给药将带来潜在毒副作用,目前临床应用仍受到限制。
细胞外囊泡(Extracellular vesicles, EVs)是一种细胞分泌的天然纳米囊泡,具有免疫原性低、生物安全性高、可穿过血脑屏障等优点。近年来,基于EVs的药物递送系统在多种疾病的治疗研究中受到广泛关注,并显示出一定的应用前景 。但天然未修饰EVs经系统给药后,易被巨噬细胞等清除,难以大量到达受损肾脏发挥作用,因此需要对EVs进行工程化改造以提高其体内循环时间和肾脏分布。
内源性配体结合是一种改善药物药代动力学的有效手段。作为一种高丰富血液蛋白,白蛋白(ALB)具有较长的体内半衰期,因此药物或纳米粒与ALB结合可延长其循环时间。此外,ALB衍生的肽段或片段具有较高的肾脏亲和力,可作为肾靶向配体。通过基因工程技术对EVs供体细胞进行改造,将目标肽段或蛋白等与EVs跨膜蛋白融合表达,从而使细胞分泌产生表面展示有目标分子的工程化EVs。该方法具有较高特异性和效率,对EVs的稳定性影响较小等优势。
在本研究中,研究团队通过基因工程技术构建表面展示有白蛋白结合肽段(ABP)的EVs,提升其体内循环时间和肾脏分布,从而增强其药物递送效率和对肾损伤的治疗效果(图1)。白蛋白结合肽段与EVs跨膜蛋白Lamp2b的融合表达质粒(ABP-Lamp2b)转染EVs供体细胞后,可产生表面展示ABP的EVs(ABP-EVs)。与未修饰EVs相比,ABP-EVs显示出类似形貌、粒径和Zeta电势等性质,但具有白蛋白结合能力。经静脉注射后,ABP-EVs在体内的循环时间长于NC-EVs,且在正常和肾损伤模型小鼠的肾脏驻留率均高于NC-EVs。进一步研究提示损伤肾脏微血管渗透性改变,巨蛋白介导的胞吞作用等多种机制共同导致ABP-EVs在受损肾脏的富集。研究团队还在体内外评估了ABP-EVs递送模式药物(小分子化合物、蛋白类药物)治疗肾损伤的疗效,结果显示ABP-EVs递送可以显著提升两种药物的抗氧化、抗凋亡、抗纤维化作用和促进肾损伤修复潜能。本研究提示ABP-EVs可能作为多功能药物载体用于治疗多种肾脏疾病,提升药物的治疗指数;内源性配体结合是工程化构建器官靶向性EVs的新思路。
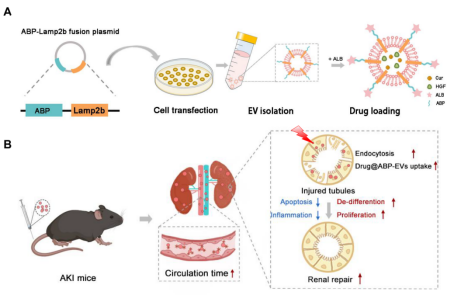
图1 ABP-EV构建及其提升药物治疗肾脏疾病疗效的模式图
该文通讯作者为刘敬平研究员,第一作者为该移植免疫研究室刘书云助理研究员。该研究得到了国家自然科学基金、华西医院1.3.5项目、四川大学博士后基金及华西医院博士后基金等的资助。
文章链接:https://www.sciencedirect.com/science/article/pii/S0168365922007611